Przegląd Mleczarski 3/2026 – Od naturalnych bioaktywnych składników do żywności projektowanej: rola produktów mleczarskich we wspieraniu funkcjonowania mózgu

Starzenie się populacji stało się jednym z najważniejszych zjawisk demograficznych XXI wieku, a jego bezpośrednią konsekwencją jest rosnąca liczba osób z zaburzeniami funkcji poznawczych.
W 2020 roku na świecie żyło ponad 55 milionów osób z demencją, a prognozy wskazują, że liczba ta może wzrosnąć do 78 milionów w 2030 roku i 139 milionów w 2050 roku [1]. Oznacza to ponad 10 milionów nowych przypadków rocznie. Coraz większy odsetek chorych będzie mieszkał w krajach o niskim i średnim dochodzie, gdzie systemy opieki zdrowotnej już dziś funkcjonują pod znaczną presją [1].Mózg w starzejącym się społeczeństwie
Szczególną uwagę zwraca łagodne zaburzenie poznawcze (MCI), uznawane za stan pośredni między fizjologicznym starzeniem się a otępieniem klinicznym. Charakteryzuje się ono deficytami poznawczymi, które nie zaburzają jeszcze istotnie samodzielnego funkcjonowania, lecz wiążą się z podwyższonym ryzykiem progresji do demencji [3]. Metaanaliza obejmująca ponad 670 tysięcy osób wykazała, że MCI dotyczy blisko 20% populacji powyżej 50. roku życia. W części badań wskazuje się również na wzrost częstości zaburzeń poznawczych po 2019 roku, co wiązano między innymi z następstwami pandemii COVID-19 [2].
Mimo postępu w neurologii i farmakologii nie dysponujemy obecnie terapią, która skutecznie zapobiegałaby rozwojowi choroby Alzheimera lub odwracała jej przebieg. Stosowane inhibitory cholinoesterazy oraz memantyna łagodzą objawy w zaawansowanych stadiach, lecz nie zatrzymują procesu neurodegeneracyjnego. Jednocześnie raport opublikowany w Lancet wskazuje, że około 45% przypadków demencji można by opóźnić lub uniknąć poprzez modyfikację 14 czynników ryzyka, tj.: nadciśnienia tętniczego, otyłości, cukrzycy, braku aktywności fizycznej, palenia tytoniu czy izolacji społecznej [1].Szczególne znaczenie przypisuje się kontroli ciśnienia tętniczego w wieku średnim, która zmniejsza ryzyko otępienia naczyniowego i może redukować ogólne ryzyko demencji [1].
W tym świetle rośnie zainteresowanie interwencjami niefarmakologicznymi, w tym rolą diety. Pytanie, czy codzienne wybory żywieniowe mogą wpływać na procesy, takie jak stres oksydacyjny, neurozapalenie czy dysfunkcja bariery jelitowej, stało się jednym z istotnych kierunków badań nad prewencją zaburzeń poznawczych [4]. Coraz wyraźniej odróżnia się przy tym tradycyjną żywność funkcjonalną od koncepcji żywności projektowanej.
Żywność funkcjonalna to produkty, które poza podstawową wartością odżywczą wykazują dodatkowe udokumentowane działanie prozdrowotne, często dzięki wzbogaceniu w witaminy, składniki mineralne, przeciwutleniacze lub probiotyki. Żywność projektowana stanowi bardziej zaawansowane podejście. W tym modelu nie chodzi jedynie o dodanie składnika, lecz o świadome kształtowanie składu i struktury produktu w oparciu o wiedzę o mechanizmach biologicznych. Obejmuje to identyfikację określonego celu molekularnego, dobór składników o potwierdzonej biodostępności oraz zastosowanie technologii pozwalających zachować ich aktywność biologiczną w przewodzie pokarmowym.
W gerontologii koncepcja ta nabiera szczególnego znaczenia. Projektowanie żywności dla osób starszych oznacza tworzenie produktów zdolnych do oddziaływania na procesy związane ze starzeniem się mózgu, zarówno poprzez bezpośredni wpływ na metabolizm komórek nerwowych, jak i pośrednio poprzez oddziaływanie na oś jelitowo-mózgową [5]. Z uwagi na powyższe, produkty mleczne, ze względu na swoją złożoną matrycę i obecność naturalnych związków bioaktywnych, stanowią interesujący punkt wyjścia do dalszych rozważań.
Związki wspierające równowagę oksydacyjną w mózgu
Stres oksydacyjny jest jednym z najlepiej udokumentowanych mechanizmów towarzyszących starzeniu się mózgu oraz rozwojowi chorób neurodegeneracyjnych. Komórki nerwowe są szczególnie podatne na uszkodzenia oksydacyjne ze względu na wysokie zużycie tlenu oraz dużą zawartość wielonienasyconych kwasów tłuszczowych w błonach komórkowych. Kluczową rolę w ochronie przed reaktywnymi formami tlenu odgrywa glutation, podstawowy wewnątrzkomórkowy antyoksydant. Synteza glutationu zależy między innymi od dostępności L-cysteiny, aminokwasu siarkowego, który bywa czynnikiem ograniczającym ten proces [6]. Białka serwatkowe, zwłaszcza β-laktoglobulina i α-laktoalbumina, stanowią stosunkowo bogate źródło cysteiny oraz innych aminokwasów siarkowych [7]. Zwiększenie podaży biodostępnych form cysteiny może sprzyjać syntezie glutationu oraz wpływać na wybrane markery stresu oksydacyjnego. Dotychczasowe badania interwencyjne wykazywały wzrost stężenia glutationu po zwiększonej podaży białek serwatkowych, jednak ograniczona liczebność prób oraz krótki czas obserwacji nie pozwalają traktować tych wyników jako dowodu faktycznego czynnika redukcji ryzyka demencji. Należy również podkreślić, że wolna cysteina podawana doustnie jest niestabilna, łatwo ulega utlenieniu i w wyższych dawkach może wykazywać działanie niepożądane [9]. Z tego względu naturalne źródła cysteiny w postaci białek mleka mogą stanowić bezpieczniejszą formę jej dostarczania. Potencjał białek mleka nie ogranicza się jednak wyłącznie do wsparcia syntezy glutationu. W odpowiednich warunkach technologicznych, zwłaszcza podczas fermentacji i kontrolowanej hydrolizy, z białek tych mogą powstawać peptydy o zróżnicowanej aktywności biologicznej, w tym o potencjale neuromodulującym.
Peptydy o potencjale neuromodulującym
Podczas fermentacji oraz kontrolowanej hydrolizy enzymatycznej białek mleka, dochodzi do uwolnienia krótkich sekwencji peptydowych o zróżnicowanej aktywności biologicznej. Część z tych peptydów wykazuje potencjał neuromodulujący, między innymi poprzez wpływ na enzymy regulujące metabolizm neuroprzekaźników,
modulację ciśnienia tętniczego lub oddziaływanie na markery zapalne. Znaczenie fizjologiczne tych obserwacji zależy od biodostępności peptydów po trawieniu oraz od ich zdolności do oddziaływania na tkanki docelowe.
Dobór szczepów bakterii oraz parametrów fermentacji wpływa na profil powstających peptydów, ponieważ aktywność proteolityczna ma charakter szczepowy i zależy od warunków technologicznych. Oznacza to, że proces fermentacji może być wykorzystywany do modyfikowania składu biologicznie czynnych sekwencji peptydowych w produkcie.
Tabela 1 przedstawia wybrane peptydy, ich źródło w białkach mleka, proponowany mechanizm działania oraz obserwowane efekty fizjologiczne [11, 12, 13].
Bioaktywne peptydy to zwykle krótkie sekwencje, najczęściej złożone z kilku do kilkunastu aminokwasów, które stają się aktywne po uwolnieniu z kazeiny lub białek serwatkowych. Nie oznacza to jednak, że każdy produkt fermentowany ma udowodniony potencjał neuroprotekcyjny. Większość danych dotyczących konkretnych sekwencji peptydowych pochodzi z badań in vitro, modeli zwierzęcych lub krótkoterminowych badań interwencyjnych u ludzi. Z tego względu fermentowane produkty mleczne należy traktować jako element diety o możliwym potencjale wspierającym wybrane mechanizmy biologiczne, a nie jako narzędzie leczenia chorób neurodegeneracyjnych. W podobny sposób analizuje się inne frakcje mleka, w tym składniki błony kuleczek tłuszczowych, których potencjalny wpływ na funkcje mózgu jest przedmiotem badań eksperymentalnych.
Frakcja białek otoczki kuleczki tłuszczowej
W procesie produkcji masła otoczka kuleczki tłuszczowej ulega mechanicznemu uszkodzeniu, a jej fragmenty przechodzą do fazy wodnej. W efekcie maślanka powstała w procesie zmaślania śmietanki, a także frakcje uzyskiwane z niej metodami filtracji membranowej, charakteryzują się podwyższoną zawartością składników otoczek kuleczek tłuszczowych (Milk Fat Globule Membrane, MFGM) niż mleko surowe.
Tabela 1. Peptydy o potencjale neuromodulującym

MFGM zawiera złożoną mieszaninę lipidów polarnych, przede wszystkim fosfolipidów i sfingolipidów, takich jak sfingomielina i fosfatydylocholina, a także glikolipidów, w tym gangliozydów. Obecne są również białka otoczki kuleczki tłuszczowej, między innymi butyrofilina, oksydaza ksantynowa oraz mucyny. W przeciwieństwie do
zasadniczej frakcji tłuszczu mlekowego, zdominowanej przez trójglicerydy, składniki MFGM wykazują budowę zbliżoną do elementów błon komórkowych organizmu, co stanowi biologiczne uzasadnienie zainteresowania ich rolą w funkcjonowaniu układu nerwowego.
Fosfolipidy i sfingolipidy są integralnymi komponentami błon neuronów oraz osłonek mielinowych. W badaniach przedklinicznych wykazano, że suplementacja preparatami bogatymi w MFGM wpływa na ekspresję genów związanych z neuroplastycznością, w tym zwiększa poziom czynnika BDNF oraz poprawia wybrane parametry poznawcze w modelach zwierzęcych. Jak podkreślają Slykerman i in. (2024), potencjał MFGM obejmuje zarówno modulację plastyczności neuronalnej, jak i wpływ na regulację odpowiedzi zapalnej oraz funkcjonowanie osi jelito-mózg, przy czym mechanizmy te mają charakter wieloczynnikowy i zależny od składu frakcji [15] (tab. 2).
Tabela 2. Wybrane składniki MFGM oraz ich potencjał w ochronie zdrowia mózgu
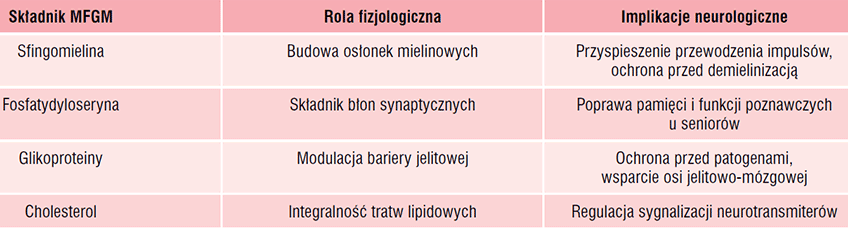
W badaniach klinicznych obserwowano poprawę wybranych funkcji poznawczych, w tym pamięci epizodycznej i funkcji wykonawczych, u osób starszych spożywających produkty wzbogacone w lipidy polarne MFGM. Jednocześnie wyniki te pozostają niejednorodne i zależą od dawki, czasu interwencji oraz sposobu pozyskania frakcji [14, 15]. Różne opracowania naukowe wskazują na znaczną zmienność składu MFGM, wynikającą z zastosowanej technologii, takiej jak mikrofiltracja czy wirowanie, co wpływa na zawartość sfingomieliny, gangliozydów oraz białek otoczki kuleczek tłuszczowych [15]. Obecny stan wiedzy pozwala traktować MFGM jako biologicznie uzasadnioną i obiecującą frakcję mleka w kontekście wspierania funkcji poznawczych. Jednocześnie konieczna jest standaryzacja preparatów oraz prowadzenie długoterminowych badań klinicznych, które umożliwią precyzyjne określenie znaczenia tej frakcji w prewencji zaburzeń neurodegeneracyjnych.
Metabolity fermentacji
Fermentacja mleka prowadzona przez bakterie kwasu mlekowego nie ogranicza się do zmiany smaku i konsystencji produktu, lecz powoduje także jego przemiany biochemiczne. W trakcie fermentacji zachodzi częściowa hydroliza białek, przekształcanie laktozy do kwasu mlekowego oraz powstawanie metabolitów, z których część wykazuje potencjalne znaczenie biologiczne, w tym oddziaływanie na mechanizmy związane z funkcjonowaniem układu nerwowego [16]. Oznacza to, że fermentacja nie tylko sprzyja powstawaniu nowych związków, ale również przekształca strukturę produktu w taki sposób, że zmienia się sposób ich uwalniania i oddziaływania w przewodzie pokarmowym. Do związków tych należą, m.in. krótkołańcuchowe kwasy tłuszczowe (maślan, propionian i octan), a także kwas γ-aminomasłowy (GABA) oraz różne peptydy sygnałowe [16]. Ich zawartość w produktach mleczarskich jest zazwyczaj niewielka i ma znaczenie raczej uzupełniające. Z punktu widzenia fizjologii, kluczowa pozostaje jednak produkcja endogenna, zależna od składu mikrobioty i podaży włókna pokarmowego. Maślan jest intensywnie badany ze względu na zdolność modulowania ekspresji genów poprzez hamowanie deacetylaz histonowych oraz wpływ na szczelność bariery jelitowej [17]. Stabilność tej bariery ma znaczenie dla ograniczenia ogólnoustrojowego stanu zapalnego, który uznaje się za jeden z czynników sprzyjających neurodegeneracji. Podobnie GABA, powstający w wyniku dekarboksylacji kwasu glutaminowego przez wybrane szczepy bakterii fermentacyjnych, jest związkiem o działaniu hamującym w ośrodkowym układzie nerwowym. GABA dostarczany z żywnością nie musi w istotnych ilościach przekraczać bariery krew-mózg, aby wywierać efekt biologiczny. Może on oddziaływać pośrednio poprzez receptory obecne w jelicie oraz modulację sygnalizacji w osi jelito-mózg [18]. Jakkolwiek, o wpływie GABA czy innych peptydów
nie decyduje wyłącznie ich obecność w produkcie, lecz również sposób, w jaki są osadzone w strukturze produktu. Właśnie matryca produktu wpływa na stabilność związku, tempo jego uwalniania w przewodzie pokarmowym oraz dostępność dla receptorów jelitowych uczestniczących w komunikacji w osi jelito-mózg.
Matryca produktu: ważna jest nie tylko zawartość składników, ale także struktura produktu
Matryca żywności to nie tylko lista składników widocznych na etykiecie, lecz sposób, w jaki są one ze sobą powiązane w gotowym produkcie. W mleku, jogurcie czy serze – białka, tłuszcze, woda i składniki mineralne tworzą określoną strukturę przestrzenną, która warunkuje właściwości fizykochemiczne i metaboliczne produktu [19]. W tej strukturze kazeina występuje w postaci miceli wiążących wapń i fosforany, tłuszcz jest zamknięty w kuleczkach z otoczką, a faza wodna stanowi środowisko dla reakcji enzymatycznych. To właśnie ta organizacja decyduje o tym, jak produkt zachowuje się w przewodzie pokarmowym.
Enzymy trawienne nie działają w sposób chaotyczny. Muszą uzyskać dostęp do określonych frakcji białka czy tłuszczu, a dostęp ten zależy od budowy produktu [20]. W jogurcie o delikatnej, żelowej strukturze, białka są już częściowo przekształcone przez fermentację, dlatego trawienie przebiega inaczej – szybciej, niż w przypadku sera dojrzewającego o zwartej konsystencji. Obróbka cieplna zmienia konformację białek poprzez denaturację i agregację, co może zwiększać podatność na działanie enzymów proteolitycznych. Z drugiej strony nadmierne przetwarzanie sprzyja reakcjom Maillarda, w których lizyna wiąże się z cukrami redukującymi, co ogranicza jej biodostępność i wartość biologiczną białka [20].
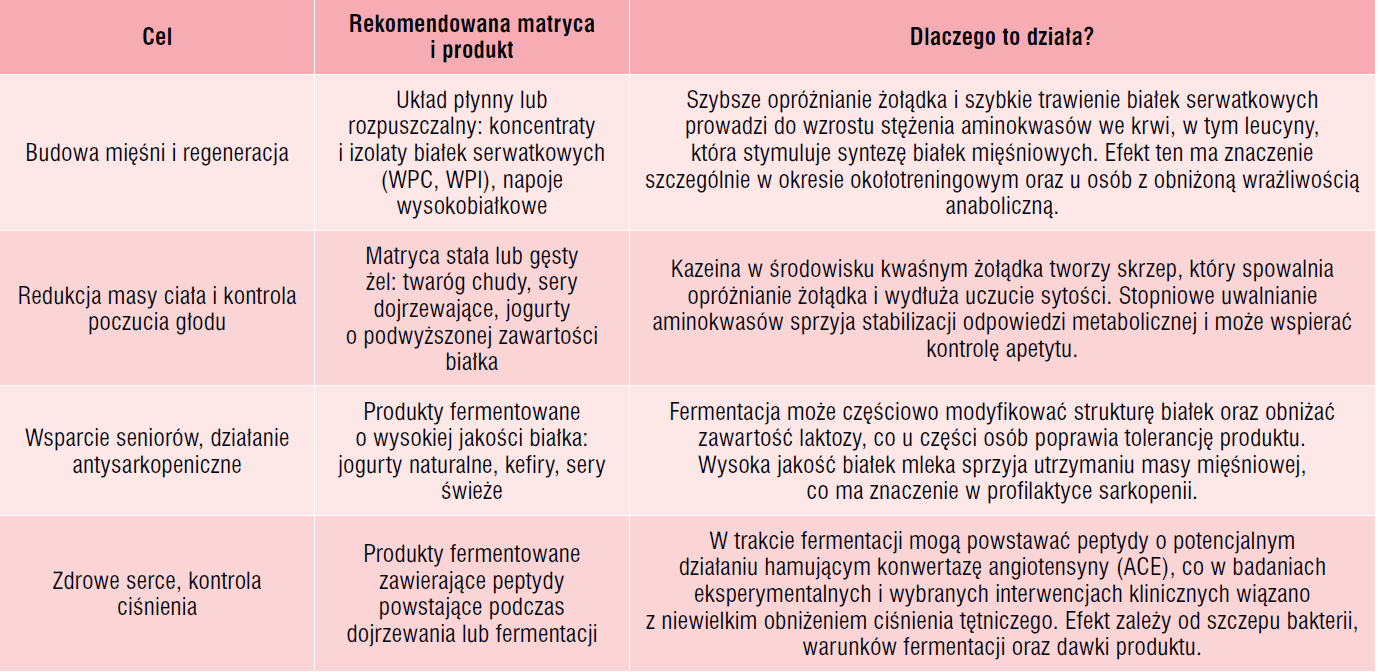
Różnice w odpowiedzi metabolicznej nie wynikają wyłącznie z ilości białka deklarowanej w produkcie, lecz również ze sposobu jego organizacji w matrycy żywności. Dwa produkty o zbliżonej zawartości białka mogą wywoływać odmienny profil wchłaniania aminokwasów. Białka serwatkowe, które nie tworzą w żołądku zwartego skrzepu, są trawione szybciej, co prowadzi do gwałtowniejszego wzrostu stężenia aminokwasów w osoczu i krótkotrwałej, intensywnej stymulacji syntezy białek mięśniowych. Kazeina natomiast ulega koagulacji w środowisku kwaśnym żołądka, tworząc strukturę spowalniającą opróżnianie treści pokarmowej i trawienie enzymatyczne. W efekcie aminokwasy są uwalniane stopniowo, co sprzyja dłuższemu utrzymaniu dodatniego bilansu azotowego. Różnice te wynikają z właściwości fizykochemicznych i strukturalnych białek oraz ich zachowania w przewodzie pokarmowym, a nie wyłącznie z profilu aminokwasowego [19].
Matryca może także pełnić funkcję ochronną wobec składników bioaktywnych. Jej struktura może ograniczać dostęp enzymów do określonych peptydów, umożliwiając ich częściowe przetrwanie w górnym odcinku przewodu pokarmowego lub przeciwnie, sprzyjać szybkiemu uwolnieniu i degradacji. Ostateczny efekt biologiczny zależy zatem, nie tylko od obecności danego związku, lecz również od sposobu w jaki został on wbudowany w strukturę produktu. W praktyce oznacza to, że zastosowana technologia przetwarzania oraz ukształtowanie struktury produktu współokreślają jego działanie metaboliczne w stopniu porównywalnym ze składem chemicznym [19, 20] (tab. 3, 4).
Tabela 3. Porównanie modeli produktów z nabiału

Tabela 4. Wybór matrycy a cel żywieniowy
Fermentacja i oś jelitowo-mózgowa
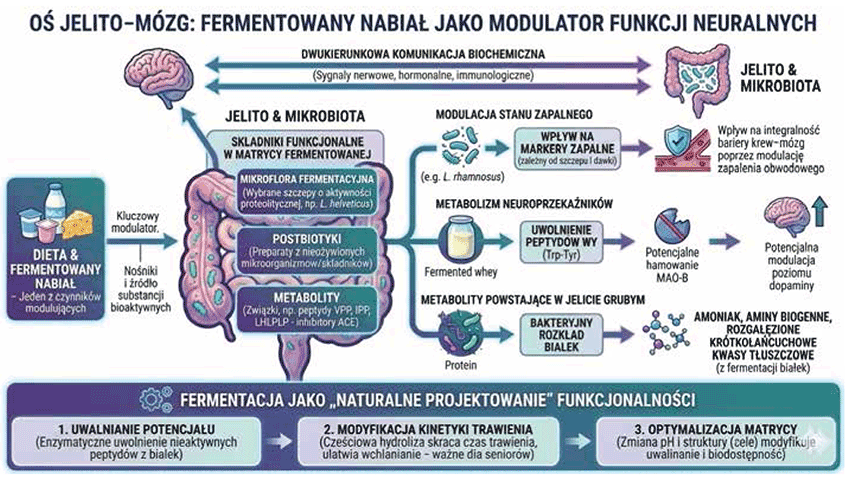
Oś jelito-mózg stanowi dwukierunkowy system komunikacji biochemicznej, integrujący sygnały nerwowe, hormonalne i immunologiczne. Dieta wpływa na elementy tej komunikacji, między innymi poprzez modyfikację składu i aktywności mikrobioty jelitowej. Produkty mleczarskie mogą oddziaływać na te mechanizmy poprzez wpływ na mikrobiotę oraz dostarczanie związków powstających w procesie fermentacji. Komunikacja w obrębie osi jelito-mózg odbywa się poprzez kilka kanałów, w których mikrobiota odgrywa istotną rolę [16]:
- Modulacja stanu zapalnego – wybrane szczepy bakterii mogą wpływać na markery zapalne i odpowiedź immunologiczną gospodarza; jednak efekt zależy od szczepu, dawki oraz przeżywalności w produkcie. Redukcja ogólnoustrojowego stanu zapalnego może sprzyjać utrzymaniu prawidłowej funkcji bariery krew-mózg, co jest istotne w mechanizmach neurozapalnych indukowanych m.in. przez lipopolisacharydy (LPS).
- Metabolizm neuroprzekaźników – mikrobiota wpływa na dostępność prekursorów neurotransmiterów. Przykładem są peptydy Trp-Tyr, np. β-laktolina uwalniana podczas fermentacji serwatki. Peptydy te w badaniach eksperymentalnych wykazywały zdolność hamowania MAO-B, co wiązano ze zwiększeniem poziomu dopaminy w tkance mózgowej [21].
- Produkty fermentacji jelitowej – w jelicie grubym zachodzi fermentacja bakteryjna składników diety, w tym białek, prowadząca do powstania amoniaku, amin biogennych oraz rozgałęzionych krótkołańcuchowych kwasów tłuszczowych. Ich profil zależy od źródła białka oraz równowagi między fermentacją białek a fermentacją węglowodanów, a ich działanie może mieć charakter zarówno korzystny, jak i niekorzystny metabolicznie.
Znaczenie ma również miejsce powstawania tych związków. Część peptydów i metabolitów tworzy się podczas fermentacji mleka, inne powstają dopiero w jelicie grubym w wyniku aktywności mikrobioty. Miejsce powstawania wpływa na to, jakie dokładnie związki dominują (na przykład inne peptydy i inne produkty rozkładu białek
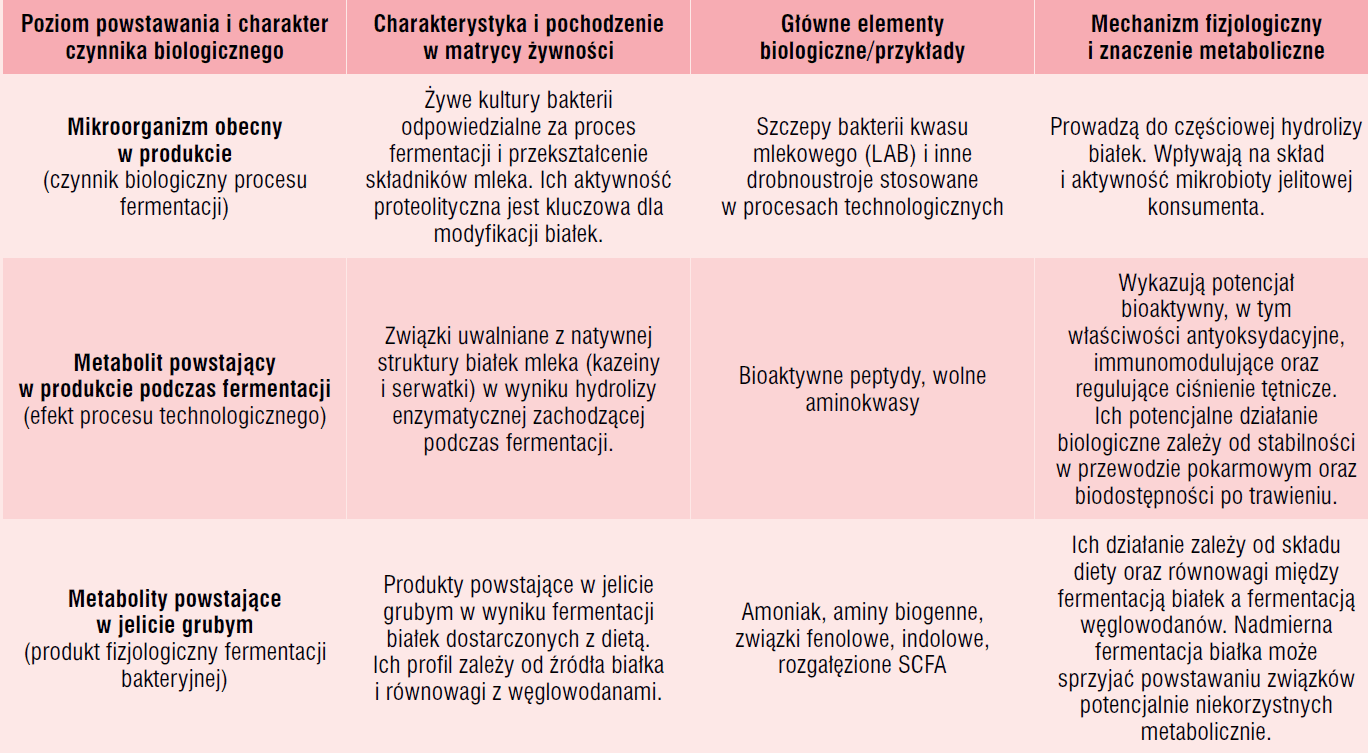
mogą powstawać w żywności, a inne w jelicie), a także na ich ilość, stabilność w przewodzie pokarmowym oraz zakres możliwego działania fizjologicznego. Rozróżnienie między mikroorganizmem obecnym w produkcie, metabolitem powstającym w trakcie fermentacji technologicznej oraz metabolitem wytwarzanym w jelicie przedstawiono w tabeli 5.
Tabela 5. Różnice między probiotykami, postbiotykami i metabolitami fermentacji
Fermentacja jest historycznie ugruntowaną, a zarazem technologicznie zaawansowaną formą naturalnego projektowania funkcjonalności produktów spożywczych.
Proces ten wykracza poza konserwację żywności:
- Uwalnia ukryty potencjał – bioaktywne peptydy pozostają nieaktywne w natywnej strukturze białek mleka; dopiero enzymatyczna aktywność bakterii prowadzi do ich uwolnienia i nadania im właściwości biologicznych [22].
- Modyfikuje kinetykę trawienia – fermentacja powoduje częściową hydrolizę białek, co może przyspieszać ich rozkład w przewodzie pokarmowym i zwiększać dostępność aminokwasów, choć efekt ten zależy od rodzaju produktu oraz stopnia przetworzenia.
- Optymalizuje matrycę – poprzez zmianę pH, przekształcenia struktury białek i tworzenie układów żelowych fermentacja modyfikuje sposób uwalniania składników odżywczych oraz biodostępność wybranych mikroelementów. W tym sensie fermentacja zmienia nie tylko skład chemiczny, lecz także strukturę produktu, która współdecyduje o jego potencjale biologicznym. Rysunek 1 ilustruje rolę fermentacji w modulowaniu komunikacji w osi jelito-mózg.
Współczesne badania wskazują, że tradycyjne produkty mleczne, takie jak jogurty naturalne, twarogi oraz wybrane sery dojrzewające, mogą stanowić istotny element żywności o potencjale funkcjonalnym, łącząc wysoką gęstość odżywczą z obecnością związków powstających w trakcie fermentacji. Takie ujęcie stanowi punkt wyjścia do dalszego rozwoju koncepcji żywności projektowanej, w której wykorzystuje się te same frakcje mleka w sposób bardziej celowy i kontrolowany.
Żywność projektowana
Zidentyfikowanie kluczowych frakcji mleka oraz mechanizmów ich oddziaływania na układ nerwowy umożliwia przejście od tradycyjnej żywności funkcjonalnej do żywności projektowanej. W tym podejściu opracowanie produktu nie ogranicza się tylko do wzbogacenia składu, lecz obejmuje świadome kształtowanie matrycy produktu oraz biodostępności wybranych związków. Proces tworzenia produktu może obejmować selektywny dobór frakcji białkowych o określonym profilu aminokwasowym, kontrolowaną hydrolizę enzymatyczną oraz celowe wzbogacanie matrycy w frakcję otoczek kuleczek tłuszczowych. Zastosowanie mikroenkapsulacji umożliwia ochronę wrażliwych peptydów i metabolitów przed degradacją. Modelowanie tekstury pozwala natomiast dostosować parametry reologiczne do potrzeb konsumentów, w tym osób z zaburzeniami połykania. W ten sposób interwencja żywieniowa może uwzględniać zarówno aspekt metaboliczny, jak i funkcjonalny związany z bezpieczeństwem spożycia. Projektowanie nie oznacza
w tym ujęciu sztucznego tworzenia nowej żywności, lecz precyzyjne wykorzystanie naturalnych składników mleka w oparciu o wiedzę o ich właściwościach biologicznych czy funkcjonalnych [23].
Ograniczenia
Pierwszym kluczowym zagadnieniem jest oddzielenie korelacji od przyczynowości. Wiele dostępnych danych pochodzi z badań obserwacyjnych, w których analizuje się zależność między spożyciem określonych produktów a częstością występowania zaburzeń poznawczych. Tego typu badania pozwalają wykrywać zależności statystyczne, lecz nie dowodzą, że dany produkt jest bezpośrednią przyczyną obserwowanego efektu. Na wyniki mogą wpływać czynniki zakłócające, takie jak poziom wykształcenia, aktywność fizyczna, status socjoekonomiczny czy ogólny styl życia. Osoby spożywające fermentowane produkty mleczne mogą jednocześnie prowadzić zdrowszy tryb życia, co utrudnia jednoznaczną interpretację wyników. Drugim istotnym elementem są różnice osobnicze w odpowiedzi metabolicznej. Reakcja organizmu na białka mleka, peptydy czy metabolity fermentacji zależy od wieku, stanu zdrowia, składu mikrobioty jelitowej oraz uwarunkowań genetycznych. To, co w jednej populacji wiąże się z poprawą wybranych parametrów poznawczych, w innej może być neutralne. Zmienność ta dotyczy również tolerancji laktozy, metabolizmu lipidów czy odpowiedzi immunologicznej. W praktyce oznacza to, że nie istnieje jeden uniwersalny model spożycia nabiału, optymalny dla wszystkich [25]. Trzecim aspektem jest znaczenie całego wzorca żywieniowego. Wzorce takie jak dieta śródziemnomorska czy modele żywienia oparte na wysokim udziale warzyw, błonnika i nienasyconych kwasów tłuszczowych są lepiej udokumentowane pod względem prewencji zaburzeń poznawczych niż pojedyncze
interwencje produktowe. Produkty mleczne mogą być elementem takiego wzorca żywieniowego [26]. Należy również uwzględnić potencjalne ograniczenia spożycia nabiału w określonych populacjach. Dotyczy to osób z nietolerancją laktozy, alergią na białka mleka krowiego, wybranymi zaburzeniami metabolicznymi czy koniecznością ograniczenia podaży sodu. W przypadku serów dojrzewających znaczenie ma zawartość soli, a w produktach deserowych zawartość cukru dodanego. Z punktu widzenia zdrowia publicznego nie można abstrahować
od tych czynników, nawet jeśli wybrane frakcje wykazują potencjał biologiczny.
Kierunki dalszego rozwoju
Dalszy rozwój koncepcji żywności ukierunkowanej na wsparcie funkcji poznawczych powinien koncentrować się na precyzyjnym łączeniu wiedzy o bioaktywnych składnikach mleka z rozwiązaniami technologicznymi zwiększającymi ich stabilność i biodostępność. Oznacza to dalsze doskonalenie metod ochrony biologicznie aktywnych peptydów, lipidów polarnych czy związków roślinnych wbudowywanych w matrycę mleczną, tak aby zachowały aktywność biologiczną w trakcie przechowywania i trawienia. Technologie, takie jak mikroenkapsulacja, mogą pełnić funkcję narzędzia wspierającego kontrolowane uwalnianie związków w jelicie, co wpisuje się w przedstawioną wcześniej koncepcję świadomego kształtowania matrycy produktu przez producenta lub dział R&D.
Drugim kierunkiem jest dostosowanie struktury i tekstury produktów mleczarskich do potrzeb osób z niepełnosprawnościami wynikającymi z wieku czy stanów chorobowych, zwłaszcza osób z zaburzeniami połykania. Modyfikacja parametrów reologicznych przy zachowaniu wysokiej gęstości odżywczej pozwala łączyć bezpieczeństwo spożycia z odpowiednią podażą białka oraz związków bioaktywnych wspierających równowagę oksydacyjną i funkcjonowanie osi jelito-mózg.
Podsumowanie
Starzenie się społeczeństw zwiększa znaczenie strategii żywieniowych wspierających utrzymanie sprawności poznawczej. W świetle dostępnych danych fermentowane produkty mleczne stanowią interesujący model żywności, w której skład chemiczny, struktura oraz proces technologiczny współdecydują o potencjale biologicznym. Białka serwatkowe, bioaktywne peptydy, składniki otoczek kuleczek tłuszczowych oraz metabolity fermentacji mogą wpływać na wybrane mechanizmy związane ze stresem oksydacyjnym, regulacją zapalną i funkcjonowaniem osi jelito-mózg. Jednocześnie większość obserwowanych efektów ma charakter pośredni lub pochodzi z badań przedklinicznych i krótkoterminowych interwencji. Nie można więc traktować pojedynczego produktu jako samodzielnego narzędzia prewencji demencji. Znaczenie ma całokształt diety, styl życia oraz indywidualne uwarunkowania metaboliczne. Koncepcja żywności projektowanej pozwala precyzyjniej wykorzystywać naturalne frakcje mleka poprzez kontrolę matrycy, tekstury produktu, strawności oraz biodostępności białek i lipidów. Jej dalszy rozwój wymaga jednak nie tylko pogłębiania wiedzy biologicznej, lecz przede wszystkim zwiększenia świadomości producentów, co do znaczenia struktury produktu w kształtowaniu odpowiedzi metabolicznej konsumenta. Niezbędne jest prowadzenie systematycznych badań technologicznych i żywieniowych na etapie projektowania wyrobów, tak aby deklarowany potencjał biologiczny był oparty na rzetelnych danych, a nie wyłącznie na ekstrapolacji wyników badań laboratoryjnych. Tylko takie podejście pozwoli na odpowiedzialne wprowadzanie produktów o ukierunkowanym działaniu do praktyki rynkowej.
mgr Julia Pucer
Katedra Mleczarstwa i Zarządzania Jakością
Wydział Nauki o Żywności
Uniwersytet Warmińsko-Mazurski w Olsztynie
dr hab. inż. Marek Aljewicz, prof. UWM
Katedra Mleczarstwa i Zarządzania Jakością
Wydział Nauki o Żywności
Uniwersytet Warmińsko-Mazurski w Olsztynie
Literatura
1. Livingston G., Huntley J., Liu K.Y., Costafreda S.G., Selbak G., Alladi S., Ames D., Banerjee S., Burns A., Brayne C., Fox N.C., Ferri C.P., Gitlin L.N., Howard R., Kales H.C., Kivimäki M., Larson E.B., Nakasujja N., Rockwood K., Samus Q., … Mukadam N. (2024). Dementia prevention, intervention, and care: 2024 report of the Lancet standing Commission.Lancet (London, England), 404(10452), 572-628. https://doi.org/10.1016/S0140-6736(24)01296-0.
2. Chen P., Cai H., Bai W., Su Z., Tang Y.L., Ungvari G.S., Ng C.H., Zhang Q. & Xiang Y.T. (2023). Global prevalence of mild cognitive impairment among older adults living in nursing homes: a meta-analysis and systematic review of epidemiological surveys. Translational psychiatry, 13(1), 88. https://doi.org/10.1038/s41398-023-02361-1.
3. Hicks A.J., Brewer J., Ahmad N., Cornelius T., Parker R.A., Dams-O’Connor K., Dickerson B., Ritchie C., Vranceanu A.M. & Bannon S.M. (2025). Dementia Care Specialists’ Perspectives of Diagnosis and Early Psychosocial Care: A Qualitative Analysis of Focus Groups in Two Large Academic Medical Centers. Journal of aging research, 2025, 3000496.
https://doi.org/10.1155/jare/3000496.
4. Mulet-Cabero A.I., Torres-Gonzalez M., Geurts J., Rosales A., Farhang B.,Marmonier C., Ulleberg E.K., Hocking E., Neiderer I., Gandolfi I., Anderson L., Brader L., Vermaak M., Cameron M., Myrup Christensen M., Haryono R. &
Peters S. (2024). The Dairy Matrix: Its Importance, Definition, and Current Application in the Context of Nutrition and Health. Nutrients, 16(17), 2908. https://doi.org/10.3390/nu16172908.
5. Cao L., Jha S.K., Gupta N., Chen X., Soni R., Yuan L., Srivastava R. & Chen Z.S. (2025). The Aging Gut-Brain Axis: Effects of Dietary Polyphenols and Metal Exposure. Chronic diseases and translational medicine, 11(4), 251-268. https://doi.org/10.1002/cdt3.70026.
6. Mandal P.K., Saharan S., Tripathi M. & Murari G. (2015). Brain glutathione levels-a novel biomarker for mild cognitive impairment and Alzheimer’s disease. Biological psychiatry, 78(10), 702-710. https://doi.org/10.1016/j. biopsych.2015.04.005.
7. Suzuki R., Arai S., Kurimoto M., Yuda N. & Tanaka M. (2025). Antioxidant Properties of Whey Protein-Derived Peptides: Radical Scavenging and Cytoprotective Effects. Food science & nutrition, 13(10), e71092. https://doi.org/10.1002/fsn3.71092.
8. Tardiolo G., Bramanti P. & Mazzon E. (2018). Overview on the Effects of N-Acetylcysteine in Neurodegenerative Diseases. Molecules (Basel, Switzerland), 23(12), 3305. https://doi.org/10.3390/molecules23123305.
9. Li F., He R., Yue Z., Yi H., Lu L., Zhang L., Shi J., Zheng C., Jiao J., Peng J., Li B. & Rong S. (2025). Effect of a 12-mo intervention with whey protein powder on cognitive function in older adults with mild cognitive impairment: a randomized controlled trial. The American journal of clinical nutrition, 121(2), 256-264. https://doi.org/10.1016/j.ajcnut.2024.11.019.
10. Park Y.W. & Nam M.S. (2015). Bioactive Peptides in Milk and Dairy Products: A Review. Korean journal for food science of animal resources, 35(6), 831- 840. https://doi.org/10.5851/kosfa.2015.35.6.831.
11. Kita M., Obara K., Kondo S., Umeda S. & Ano Y. (2018). Effect of Supplementation of a Whey Peptide Rich in Tryptophan-Tyrosine-Related Peptides on Cognitive Performance in Healthy Adults: A Randomized, Double-Blind, Placebo-Controlled Study. Nutrients, 10(7), 899. https://doi.org/10.3390/nu10070899.
12. Beganović J., Kos B., Leboš Pavunc A., Uroić K., Džidara P. & Šušković J. (2013). Proteolytic activity of probiotic strain Lactobacillus helveticus M92. Anaerobe, 20, 58-64. https://doi.org/10.1016/j.anaerobe.2013.02.004.
13. Phelan, M., & Kerins, D. (2011). The potential role of milk-derived peptides in cardiovascular disease. Food & function, 2(3-4), 153-167. https://doi.org/10.1039/c1fo10017c.
14. Yufeng Du., Yan Borné, Jessica Samuelsson, Isabelle Glans, Xiaobin Hu, Katarina Nägga, Sebastian Palmqvist, Oskar Hansson, Emily Sonestedt. High- and Low-Fat Dairy Consumption and Long-Term Risk of Dementia. Neurology, 2026; 106 (2) DOI: 10.1212/WNL.0000000000214343.
15. Slykerman R., Davies N., Fuad M. & Dekker J. (2024). Milk Fat Globule Membranes for Mental Health across the Human Lifespan. Foods (Basel, Switzerland), 13(11), 1631. https://doi.org/10.3390/foods13111631.
16. Schächtle M.A. & Rosshart S.P. (2021). The Microbiota-Gut-Brain Axis in Health and Disease and Its Implications for Translational Research. Frontiers in cellular neuroscience, 15, 698172. https://doi.org/10.3389/fncel.2021.698172.
17. McBride D.A., Dorn N.C., Yao M., Johnson W.T., Wang W., Bottini N. & Shah N.J. (2023). Short-chain fatty acid-mediated epigenetic modulation of inflammatory T cells in vitro. Drug delivery and translational research, 13(7),
1912-1924. https://doi.org/10.1007/s13346-022-01284-6.
18. Kim C.S. (2024). Roles of Diet-Associated Gut Microbial Metabolites on Brain Health: Cell-to-Cell Interactions between Gut Bacteria and the Central Nervous System. Advances in nutrition (Bethesda, Md.), 15(1),
100136. https://doi.org/10.1016/j.advnut.2023.10.008.
19. Aguilera J.M. (2019). The food matrix: implications in processing, nutrition and health. Critical reviews in food science and nutrition, 59(22), 3612-3629. https://doi.org/10.1080/10408398.2018.1502743.
20. Basha S., Ks P., Chattopadhyay A., Ramakrishna Pai A. & Kishore Mahato K. (2025). Emerging insights into dairy products and Alzheimer’s disease: exploring the potential neuroprotective effects. Critical reviews in food
science and nutrition, 1-28. Advance online publication. https://doi.org/10.1080/10408398.2025.2578711.
21. Fukuda T., Kanatome A., Takashima A., Tajima O., Umeda S. & Ano Y. (2022). Effect of Whey-Derived Lactopeptide β-Lactolin on Memory in Healthy Adults: An Integrated Analysis of Data from Randomized Controlled
Trials. The journal of nutrition, health & aging, 26(2), 127-132. https://doi.org/10.1007/s12603-022-1733-8.
22. Li H., Gong H., Wang J. & Mao, X. (2025). Bioactive peptides from milk proteins: current insights into novel preparation strategies and application prospects. Critical reviews in food science and nutrition, 1-19. Advance
online publication. https://doi.org/10.1080/10408398.2025.2598810.
23. Snir B.; Fishman A.; Glusac J. Chickpea-Based Milk Analogue Stabilized by Transglutaminase. Foods 2025, 14, 514.
https://doi.org/10.3390/foods14030514.
24. Popovici V.; Boldianu A.B.; Pintea A.; Caraus V.; Ghendov-Mosanu A.; Subotin I.; Druta R.; Sturza R. In Vitro Antioxidant Activity of Liposomal Formulations of Sea Buckthorn and Grape Pomace. Foods 2024, 13, 2478.
https://doi.org/10.3390/foods13162478.
25. Mills S., Stanton C., Lane J.A., Smith G.J. & Ross R.P. (2019). Precision Nutrition and the Microbiome, Part I: Current State of the Science. Nutrients, 11(4), 923. https://doi.org/10.3390/nu11040923 .
26. Cherian L., Wang Y., Fakuda K., Leurgans S., Aggarwal N. & Morris M. (2019). Mediterranean-Dash Intervention for Neurodegenerative Delay (MIND) Diet Slows Cognitive Decline After Stroke. The journal of prevention of
Alzheimer’s disease, 6(4), 267-273. https://doi.org/10.14283/jpad.2019.28.
















